
Introdução de Produto
| Informações básicas de piridina |
| Estrutura Química Propriedades químicas Produções Usos Informações sobre toxicidade Referências sobre perigos |
| Nome do Produto: | Piridina |
| Sinônimos: | ácido piridinocarboxílico,2-(4,5-dihidro-4-metil-4-(1-metiletil)-5-oxo-1h-imidazol{ {9}}il)-5-metil;piridinocarboxílicoácido,2-(4,5-dihidro-4-metil-4-(1-metiletil){{ 17}}oxo-1h-imidazol-2-il)-5-metil,sal de monoamônio;Número de resíduo Rcra U196;rcrawastenumberu196;FEMA 2932;FEMA 2966;NÚMERO FEMA 2966;azabenzeno |
| CAS: | 110-86-1 |
| MF: | C5H5N |
| PM: | 79.1 |
| EINECS: | 203-809-9 |
| Categorias de Produtos: | Frascos de vidro âmbar;NMR;Frascos de solvente;Solvente por aplicação;Solvente por tipo;Opções de embalagem de solvente;Solventes biotecnológicosSolventes;Frascos de solvente;Solventes;Claro/Selo? Frascos; Grau espectrofotométrico; Solventes espectrofotométricos; Solventes de espectroscopia (IR; UV/Vis); Organostannes; Tributilestanny; Química; PS; Classificação alfa; Voláteis/semivoláteis; Frascos de vidro âmbar; ; Solventes de Grau ACS; -Solventes a granel; Solventes de grau ACS; Latas de aço carbono com roscas NPT; Solventes de recipientes retornáveis; Solventes de grau ACS e de reagente; ReagentPlus; Produtos de grau de solvente ReagentPlus; ;Analítico/Cromatografia;Multi-Compêndio;Puriss pa;Puriss pa ACS;Frascos revestidos de PVC;Frascos de alumínio;CHROMASOLV Plus;Reagentes de cromatografia &;HPLC &;Solventes de grau HPLC Plus (CHROMASOLV);Solventes HPLC/UHPLC (CHROMASOV);UHPLC Solventes (CHROMASOLV); Solventes de grau ACS; Latas de aço carbono com roscas NPT; Solventes semi-granel; Halogenados; {{10} };bc0001 |
| Arquivo mol: | 110-86-1.mol |
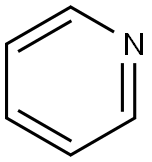 |
|
| Propriedades Químicas da Piridina |
| Ponto de fusão | -42 grau (lit.) |
| Ponto de ebulição | 115 graus (aceso.) |
| densidade | 00,978 g/mL a 25 graus (lit.) |
| densidade do vapor | 2,72 (vs ar) |
| pressão de vapor | 23,8 mm Hg (25 graus) |
| índice de refração | n20/D 1.509(lit.) |
| FEMA | 2966|PIRIDINA |
| Fp | 68 graus F |
| temperatura de armazenamento. | Armazene em +5 grau até +30 grau. |
| solubilidade | H2O: de acordo |
| PKA | 5,25 (a 25 graus) |
| forma | Líquido |
| cor | incolor |
| Odor | Odor nauseante detectável em 00,23 a 1,9 ppm (média=00,66 ppm) |
| Polaridade relativa | 0.302 |
| PH | 8,81 (H2O, 20 graus) |
| limite explosivo | 12.4% |
| Limiar de odor | 0,063 ppm |
| Tipo de odor | duvidoso |
| Solubilidade em água | Miscível |
| Ponto de congelamento | -42 grau |
| λmax | λ: 305 nm Amáx: 1.00 λ: 315 nm Amáx: 0,15 λ: 335 nm Amáx: 0,02 λ: {{0}} nm Amáx: 0,01 |
| Merck | 14,7970 |
| BRN | 103233 |
| Constante da Lei de Henry | 18,4 a 30 graus (headspace-GC, Chaintreau et al., 1995) |
| Limites de exposição | TLV-TWA 5 ppm (-15 mg/m3) (ACGIH, MSHA e OSHA); STEL 10 ppm (ACGIH), IDLH 3600 ppm (NIOSH). |
| Constante dielétrica | 12,5 (20 graus) |
| Estabilidade: | Estábulo. Inflamável. Incompatível com agentes oxidantes fortes, ácidos fortes. |
| InChIKey | JUJWROOIHBZHMG-UHFFFAOYSA-N |
| LogP | 00,64 a 20 graus |
| Referência de banco de dados CAS | 110-86-1(Referência do banco de dados CAS) |
| Referência Química do NIST | Piridina(110-86-1) |
| IARC | 2B (Vol. 77, 119) 2019 |
| Sistema de registro de substâncias da EPA | Piridina (110-86-1) |
| Informação de Segurança |
| Códigos de perigo | T,N,F,Xn |
| Declarações de Risco | 11-20/21/22-39/23/24/25-23/24/25-52-36/38 |
| Declarações de segurança | 36/37/39-38-45-61-28A-26-28-24/25-22-36/37-16-7 |
| OEB | A |
| OEL | TWA: 5 ppm (15 mg/m3) |
| RIDADR | ONU 1282 3/PG 2 |
| WGK Alemanha | 2 |
| RTECS | UR8400000 |
| F | 3-10 |
| Temperatura de autoignição | 482 graus |
| Nota de perigo | Altamente inflamável/prejudicial |
| TSCA | Sim |
| Código HS | 2933 31 00 |
| Classe de Perigo | 3 |
| Grupo de embalagem | II |
| Dados sobre substâncias perigosas | 110-86-1(dados de substâncias perigosas) |
| Toxicidade | LD50 por via oral em ratos: 1,58 g/kg (Smyth) |
| IDLA | 1,000 ppm |
| Informações MSDS |
| Fornecedor | Linguagem |
|---|---|
| Sigma Aldrich | Inglês |
| ACROS | Inglês |
| ALFA | Inglês |
| Uso e síntese de piridina |
| Estrutura química | A piridina é um composto orgânico heterocíclico básico com a fórmula química C5H5N. Está estruturalmente relacionado ao benzeno, com um grupo metino (=CH−) substituído por um átomo de nitrogênio. O anel piridínico ocorre em muitos compostos importantes, incluindo azinas e as vitaminas niacina e piridoxina.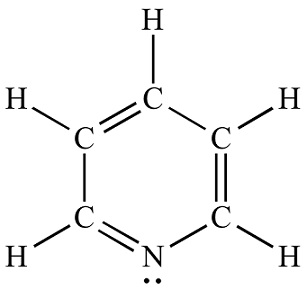 Estrutura de Piridina Lewis |
| Propriedades quimicas | A piridina é um líquido incolor e inflamável com um odor forte e desagradável de peixe. Piridina |
| Produções | 2.1 Separação do Alcatrão As bases piridina são constituintes do alcatrão. Eles foram isolados do alcatrão ou do gás de carvão antes que os processos de fabricação sintética fossem estabelecidos. As quantidades contidas no alcatrão e no gás de carvão são pequenas e as bases piridina isoladas deles são uma mistura de muitos componentes. Assim, com algumas exceções, o isolamento de bases piridínicas puras era caro. Hoje, quase todas as bases de piridina são produzidas por síntese.2.2 Síntese de chichibabina 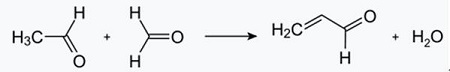 Figura 2-1Formação de acroleína a partir de acetaldeído e formaldeído 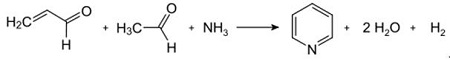 Figura 2-2Condensação de piridina a partir de acroleína e acetaldeído A síntese da piridina Chichibabin foi relatada em 1924 e ainda é usada na indústria. O acetaldeído e o formaldeído reagem com a amônia para formar principalmente piridina. Primeiro, a acroleína é formada em uma condensação Knoevenagel a partir do acetaldeído e do formaldeído. É então condensado com acetaldeído e amônia em di-hidropiridina e depois oxidado com um catalisador de estado sólido em piridina. A reação geralmente é realizada a 350-550°C e a uma velocidade espacial de 500-1000 h-1na presença de um catalisador ácido sólido (por exemplo, sílica-alumina). O produto consiste em uma mistura de piridina, piridinas metiladas simples (picolina) e lutidina. A piridina recuperada é separada dos subprodutos em um processo de vários estágios. 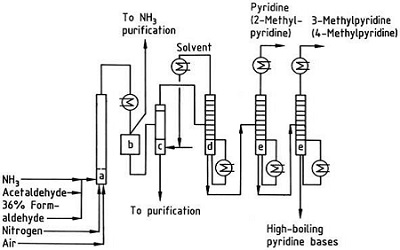 Figura 2-3Fluxograma de produção de piridina e metilpiridina a partir de acetaldeído e formaldeído com amônia. A) Reator; b) Colecionador; c) Extração; d) Destilação de solvente; e) Destilação 2.3 Desalquilação de Alquilpiridinas A piridina pode ser preparada por desalquilação de piridinas alquiladas, que são obtidas como subprodutos na síntese de outras piridinas. A desalquilação oxidativa é realizada usando ar sobre catalisador de óxido de vanádio (V), por desalquilação a vapor em catalisador à base de níquel ou hidrodesalquilação com um catalisador à base de prata ou platina. Rendimentos de piridina de até 93% podem ser alcançados com o catalisador à base de níquel. 2.4 Síntese de Nitrilas e Acetileno A reação em fase líquida de nitrilas com acetileno é realizada a 120-180 ?C e 0.8-2,5 MPa na presença de um catalisador organocobalto e dá 2-piridinas substituídas : 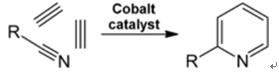 Figura 2-4Síntese de 2-metilpiridina a partir de nitrilas e acetileno A trimerização de uma parte de uma molécula de nitrila e duas partes de acetileno em piridina é chamada de ciclização de Bönnemann. Ao usar acetonitrila como nitrila, obtém-se 2-metilpiridina, que pode ser desalquilada em piridina. 2.5 Síntese de Acrilonitrila e Cetonas 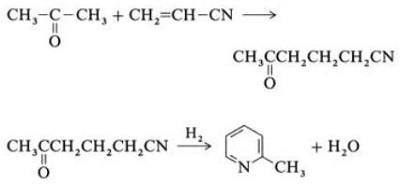 Figura 2-5Síntese de 2-metilpiridina a partir de acrilonitrila e acetona A síntese de acrilonitrila e acetona fornece 2-metilpiridina seletivamente, que pode ser desalquilada em piridina. Primeiro, a reação de acrilonitrila e acetona, catalisada por uma amina alifática primária, como a isopropilamina, e um ácido fraco, como o ácido benzóico, ocorre na fase líquida a 180 ºC e 2,2 MPa para dar 5-oxohexanonitrila, com 91 % seletividade. A conversão de acrilonitrila é de 86%. Em seguida, a ciclização e a desidratação do produto inicial são realizadas na fase gasosa na presença de hidrogênio sobre um catalisador contendo paládio, níquel ou cobalto a 240°C para fornecer 2-metilpiridina com rendimento de 84%. 2.6 Síntese de Dinitrilas Em uma reação em fase de vapor sobre um catalisador contendo níquel na presença de hidrogênio, 2-metilglutaronitrila dá 3-metilpiperidina, que então sofre desidrogenação sobre paládio –alumina para dar 3-metilpiridina. E a 3-metilpiridina também pode ser desalquilada em piridina. 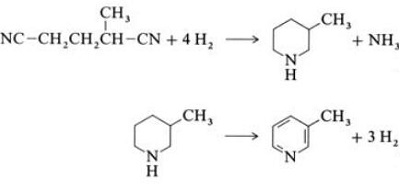 Figura 2-6Síntese de 2-metilpiridina a partir de dinitrilas É relatado que uma reação em fase gasosa de uma etapa sobre um catalisador contendo paládio fornece 3-metilpiridina com rendimento de 50%. 2.7 Biossíntese Vários derivados de piridina desempenham papéis importantes em sistemas biológicos. Embora a sua biossíntese não seja totalmente compreendida, o ácido nicotínico (vitamina B3) ocorre em algumas bactérias, fungos e mamíferos. Os mamíferos sintetizam o ácido nicotínico através da oxidação do aminoácido triptofano, onde um produto intermediário, a anilina, cria um derivado da piridina, a quinurenina. Pelo contrário, as bactérias Mycobacterium tuberculosis e Escherichia coli produzem ácido nicotínico por condensação de gliceraldeído 3-fosfato e ácido aspártico. 2.8 Outros métodos O etileno e a amônia reagem na presença de um catalisador complexo de paládio para dar 2-metilpiridina e MEP. A piridina pode ser preparada a partir de ciclopentadieno por amoxidação ou de 2-pentenonitrila por ciclização e desidrogenação. O álcool furfurílico ou furfural reage com a amônia na fase gasosa para dar piridina. 2-A metilpiridina também é preparada a partir da anilina. |
| Usos | 3.1 Solvente A piridina (110-86-1) é um solvente polar, básico e de baixa reatividade, especialmente para reações de desidrocloração e extração de antibióticos. Na reação de eliminação, a piridina atua como base da reação de eliminação e liga o haleto de hidrogênio resultante para formar um sal de piridínio. Nas esterificações e acilações, a piridina ativa os haletos ou anidridos do ácido carboxílico. 3.2 Medicamentos A estrutura química da piridina pode ser encontrada em vários medicamentos que são sintetizados, em parte, graças à piridina. Um exemplo é um medicamento chamado esomeprazol, o nome genérico do Nexium. Este é um medicamento usado para tratar a DRGE, ou doença do refluxo gastroesofágico. Outro exemplo de medicamento contendo piridina é a loratadina, mais comumente conhecida por sua marca Claritin. Loratadina auxilia no tratamento de alergias. 3.3 Pesticidas O principal uso da piridina é como precursor dos herbicidas paraquat e diquat. A primeira etapa de síntese do inseticida clorpirifós consiste na cloração da piridina. A piridina também é o composto inicial para a preparação de fungicidas à base de piritiona. O cetilpiridínio e o laurilpiridínio, que podem ser produzidos a partir da piridina com reação de Zincke, são usados como anti-sépticos em produtos de higiene bucal e odontológica. A piridina é facilmente atacada por agentes alquilantes para formar sais de N-alquilpiridínio. Um exemplo é o cloreto de cetilpiridínio.  Fig 3-1 Síntese de paraquat 3.4 Síntese de piperidina A piperidina, um heterociclo fundamental do nitrogênio, é um importante componente sintético. As piperidinas são produzidas pela hidrogenação da piridina com um catalisador à base de níquel, cobalto ou rutênio em temperaturas elevadas. C5H5N + 3 H2 → C5H10NH3.5 Ligante e base de Lewis A piridina é amplamente utilizada como ligante na química de coordenação. Como ligante de complexo metálico, pode ser facilmente substituído por uma base de Lewis mais forte, que pode ser utilizada na catálise de reações de polimerização e hidrogenação. Após a conclusão da reação, o ligante piridina substituído durante a reação pode ser restaurado novamente. A piridina também é usada como base em reações de condensação. Como base, a piridina pode ser utilizada como reagente de Karl Fischer, mas costuma ser substituída por alternativas de odor mais agradável, como o imidazol. 3.6 Outros Exceto para os usos acima, a Piridina também é usada para produzir resinas de policarbonato, vitaminas, aromatizantes de alimentos, tintas, corantes, produtos de borracha, adesivos e impermeabilizantes para tecidos. A piridina é adicionada ao etanol para torná-lo impróprio para beber. Também é usado na síntese in vitro de DNA. |
| Informações sobre toxicidade | 4.1 Nível de Toxicidade Baixa Toxicidade 4.2 Toxicidade Aguda LD501580mg/kg (ratos grandes, oral); 1121mg/kg (Coelho, através da pele); inalado por humanos 25mg/m3×20 min, irritação da conjuntiva e da mucosa do trato respiratório superior. Toxicidade subaguda e crônica: inalado por camundongos grandes 32,3mg/m3×7 horas/dia x5 dias/semana x6 meses, aumento do peso do fígado; inalado por humanos 20-40mg/m3 (longo prazo), danos nos nervos, caminhada instável, tremores digitais, pressão arterial baixa, suor excessivo, danos ocasionais no fígado e nos rins. |
| Perigos | 5.1 Perigos para a saúde A piridina é extremamente tóxica por ingestão e inalação. Vapores são mais pesados que o ar. sua combustão produz óxidos tóxicos de nitrogênio. A piridina é altamente inflamável (seu ponto de inflamação é de apenas 17 ºC). A piridina também pode ter efeitos neurotóxicos e genotóxicos. 5.2 Riscos de Incêndio Comportamento em caso de incêndio: O vapor é mais pesado que o ar e pode percorrer distâncias consideráveis até a fonte de ignição e gerar chama. |
| Referências |
https://en.wikipedia.org/wiki/Piridina#Ocorrência http://www.zwbk.org/MyLemmaShow.aspx?zh=zh-tw&lid=169038 http://www.softschools.com/formulas/química/piridina_formula/378/ http://www.hmdb.ca/metabolites/HMDB0000926 https://study.com/academy/lesson/pyridine-in-medicine-uses-synthesis.html#partialRegFormModal http://www.toxipedia.org/display/toxipedia/Piridina https://www.chemicalbook.com/ProductChemicalPropertiesCB8852825_EN.htm https://pubchem.ncbi.nlm.nih.gov/compound/pyridine#section=Principal http://www.ebi.ac.uk/chebi/searchId.do;jsessionid=E7088896622D62FC650863C2AD197CAA?chebiId=CHEBI:16227 https://www.britannica.com/science/piridina Shimizu, S.; Watanabe, N.; Kataoka, T.; Shoji, T.; Abe, N.; Morishita, S.; Ichimura, H. (2005), "Piridina e Derivados de Piridina", Enciclopédia de Química Industrial de Ullmann, Weinheim: Wiley-VCH, doi:10.1002/14356007.a22_399 |
| Propriedades quimicas | Piridina, é um líquido ligeiramente amarelo ou incolor; higroscópico; odor desagradável; gosto ardente; reação ligeiramente alcalina; solúvel em água, álcool, éter, benzeno e óleos graxos; gravidade específica, 0,978; temperatura de autoignição, 482 graus. A piridina, uma amina terciária, é uma base um pouco mais forte que a anilina e forma facilmente sais de amônio quaternário. |
| Propriedades quimicas | A piridina é uma base fraca (pKa{{0}}.25); uma solução 0,2 M tem um pH de 8,5 (HSDB 1988). Seus átomos de carbono são desativados para substituição eletrofílica. Isto é especialmente verdadeiro em meios ácidos, onde os sais se formam no nitrogênio. No entanto, sofre prontamente substituição nucleofílica, preferencialmente na posição C-2 e também na posição C-4 (Jori et al 1983). Por ser uma amina terciária, a piridina reage com agentes alquilantes para formar sais quaternários (Santodonato et al 1985). Devido à sua reduzida capacidade de doar elétrons, é mais resistente à oxidação que o benzeno. A oxidação com peróxidos forma N-óxido de piridina que é então capaz de sofrer substituição eletrofílica (Jori et al 1983). A piridina reage violentamente com vários compostos, incluindo ácido nítrico, ácido sulfúrico, anidrido maleico, percromato, beta-propiolactona e ácido clorossulfônico. A decomposição térmica pode liberar cianetos (Gehring 1983). Tanto o íon piridínio quanto a própria piridina são facilmente reduzidos ao composto comercialmente importante, a piperidina (Jori et al 1983). |
| Propriedades físicas | Líquido límpido, incolor a amarelo pálido, inflamável, com odor pungente, penetrante e nauseante de peixe. As concentrações limiares de odor na água e no ar foram de 2 ppm (Buttery et al., 1988) e 21 ppbv(Leonardos et al., 1969), respectivamente. Concentrações limite de detecção de odor de 00,74 mg/m3(2,3 ppmv) e 6 mg/m3(1,9 ppmv) foram determinados experimentalmente por Katz e Talbert (1930) e Dravnieks (1974), respectivamente. Cometto-Mučiz e Cain (1990) relataram uma concentração média de limiar de pungência nasal de 1.275 ppmv. |
| Ocorrência | A piridina foi descoberta por Anderson no alcatrão de carvão em 1846 (Windholz et al 1983). É encontrado na fumaça do tabaco (Vohl e Eulenberg 1871; Lehmann 1909) e no café torrado (Bertrand e Weisweiller 1913). A piridina é encontrada no óleo de madeira e nas folhas e raízes de Atropa belladonna (HSDB 1988), e também é um componente do óleo de creosoto (Krone et al 1986). Na natureza, a piridina e seus derivados são comumente encontrados como componentes de alcalóides, vitaminas e coenzimas. |
| Usos | A piridina é usada como solvente nas indústrias de tintas e borracha; como intermediário em corantes e produtos farmacêuticos; para desnaturar álcool; e como reagente para análise de cianeto. Ocorre no alcatrão de carvão. |
| Usos | A piridina é usada diretamente na desnaturação de álcool (ACGIH 1986; HSDB 1989; NSC 1978) e como solvente na preparação de tintas e borracha (ACGIH 1986; HSDB 1989; NSC 1978) e em laboratórios de pesquisa para funções como extração de hormônios vegetais ( Santodonato et al. Metade da piridina produzida hoje é usada como intermediário na fabricação de vários inseticidas e herbicidas para aplicações agrícolas (ACGIH 1986; Harper et al. 1985; Santodonato et al. 1985). Aproximadamente 20% vai para a produção de piperidina (Harper et al. 1985; Santodonato et al. 1985), que é comercialmente significativa na preparação de produtos químicos utilizados na vulcanização da borracha e na agricultura (NSC 1978). A piridina também é usada como intermediário na preparação de medicamentos (anti-histamínicos, esteróides, sulfas e outros agentes antibacterianos), corantes, repelentes de água e resinas de policarbonato (ACGIH 1986; Harper et al. 1985; NSC 1978; Santodonato et al. 1985). A piridina também é aprovada pela Food and Drug Administration (FDA) para uso como agente aromatizante na preparação de alimentos (Harper et al. 1985; HSDB 1989). |
| Definição | ChEBI: A piridina é um azaareno que compreende um núcleo de benzeno no qual um grupo -CH é substituído por um átomo de nitrogênio. É o composto original da classe das piridinas. As moléculas possuem um anel hexagonal planar e são isoeletrônicas com o benzeno. A piridina é um exemplo de composto heterocíclico aromático, com os elétrons nas ligações pi carbono-carbono e o par solitário de nitrogênio deslocalizado sobre o anel de átomos. O composto é extraído do alcatrão de carvão e utilizado como solvente e matéria-prima para síntese orgânica. |
| Métodos de produção | A piridina é produzida a partir de gases obtidos pela coqueificação do carvão e por síntese direta. A fração de óleo leve do alcatrão de carvão é tratada com ácido sulfúrico para produzir sais de piridina solúveis em água e então as bases de piridina são recuperadas da fase aquosa por hidróxido de sódio ou amônia (Jori et al 1983). A maior parte da produção dos EUA é feita por meios sintéticos. Este processo utiliza uma reação em fase de vapor de acetaldeído, formaldeído e amônia, que produz uma mistura de piridina e 3-metilpiridina (Santodonato et al 1985). A proporção do produto depende das quantidades relativas de acetaldeído e formaldeído. A adição de metanol aumenta o rendimento. A produção de piridina nos EUA foi estimada em 32 a 47 milhões de libras em 1975 (Reinhardt e Brittelli 1981). A piridina está disponível comercialmente em graus técnicos, 2 graus e 1 grau, sendo os dois últimos referentes às suas faixas de ebulição. As impurezas principais são homólogos de maior ponto de ebulição, como picolinas, lutidinas e colidinas, que são mono-, di- e trimetilpiridinas (Santodonato et al 1985; Jori et al 1983). |
| Preparação | A piridina é produzida por isolamento de fontes naturais, como o carvão, ou por síntese química (HSDB 1989). A piridina é produzida pela destilação fracionada de resíduos de alcatrão de carvão (HSDB 1989; NSC 1978; Santodonato et al. 1985) em que 1 tonelada de carvão produz 0.07-00,21 libras de bases de piridina de dos quais 57% é piridina (Santodonato et al, 1985). A piridina produzida sinteticamente é atualmente a fonte mais importante de piridina para usos comerciais (Santodonato et al. 1985). Pequenas quantidades de piridina são sintetizadas a partir de acetaldeído, formaldeído e amônia com um catalisador fluidizado de sílica-alumina, seguido de fracionamento para isolar a piridina (Harper et al. 1985; HSDB 1989; NSC 1978). A piridina é produzida a partir de fontes naturais pela Crowley Tar Products de Stow, Ohio, e Oklahoma City, Oklahoma (Harper et al. 1985; HSDB 1989; SRI 1986, 1987, 1988). A piridina é produzida sinteticamente por duas empresas, a Nepera Chemical Co. de Harriman, Nova York e a Reilly Tar and Chemical Corporation de Indianápolis, Indiana (Harper et al. 1985; SRI 1986, 1987, 1988). |
| Valores limite de aroma | Detecção: 0,079 a 790 ppb; reconhecimento: 7,9 a 40 ppm |
| Descrição geral | Líquido límpido, incolor a amarelo claro, com odor penetrante e nauseante. Densidade 0,978 g/cm3. Ponto de inflamação 68 graus F. Os vapores são mais pesados que o ar. Tóxico por ingestão e inalação. A combustão produz óxidos tóxicos de nitrogênio. |
| Reações do Ar e da Água | Altamente inflamável. Solúvel em água. |
| Perfil de reatividade | O azabenzeno é uma base. Reage exotérmicamente com ácidos. Durante a preparação de um complexo de Azabenzeno com trióxido de cromo, um ácido, a proporção de trióxido de cromo foi aumentada. O aquecimento desta reação ácido-base levou a uma explosão e incêndio [Histórico de caso MCA 1284 1967]. Uma solução de 0,1% de azabenzeno (ou outra amina terciária) em anidrido maleico a 185 graus dá uma decomposição exotérmica com rápida evolução de gás [Chem Eng. Notícias 42(8); 41 1964]. A mistura de Azabenzeno em porções molares iguais com qualquer uma das seguintes substâncias em um recipiente fechado fez com que a temperatura e a pressão aumentassem: ácido clorossulfônico, ácido nítrico (70%), oleum, ácido sulfúrico (96%) ou propiolactona [NFPA 1991]. A combinação de iodo, azabenzeno, trióxido de enxofre e formamida desenvolveu um gás sobre pressurização após vários meses. Isto surgiu da lenta formação de ácido sulfúrico a partir da água externa ou da desidratação da formamida em cianeto de hidrogênio. O óxido de etileno e o SO2 podem reagir violentamente na solução de Azabenzeno com pressurização se o óxido de etileno estiver em excesso (Nolan, 1983, Case History 51). |
| Perigo | Inflamável, risco de incêndio perigoso, limites de explosão no ar 1,8–12,4%. Tóxico por ingestão e inalação. Irritante para a pele, danos ao fígado e aos rins. Carcinógeno questionável. |
| Perigo à saúde | A toxicidade aguda da piridina é baixa. A inalação causa irritação do sistema respiratório e pode afetar o sistema nervoso central, causando dor de cabeça, náusea, vômito, tontura e nervosismo. A piridina irrita os olhos e a pele e é facilmente absorvida, causando efeitos sistêmicos. A ingestão de piridina pode resultar em danos ao fígado e aos rins. A piridina causa fadiga olfativa e seu odor não fornece um aviso adequado sobre a presença de concentrações prejudiciais. A piridina não foi considerada cancerígena ou apresenta toxicidade reprodutiva ou de desenvolvimento em humanos. A exposição crônica à piridina pode resultar em danos ao fígado, rins e sistema nervoso central. |
| Perigo à saúde | Os efeitos tóxicos da piridina incluem dor de cabeça, tontura, nervosismo, náusea, insônia, micção frequente e dor abdominal. Os sintomas foram transitórios, ocorreram em pessoas devido à exposição subaguda a vapores de piridina a cerca de 125 ppm durante 4 horas por dia durante 1–2 semanas (Reinhardt e Brittelli 1981). Os órgãos-alvo da toxicidade da piridina são o sistema nervoso central, o fígado, os rins, o trato gastrointestinal e a pele. As vias de exposição são a inalação de vapores e a ingestão e absorção do líquido pela pele. Sérios riscos à saúde podem surgir da inalação crônica, que pode causar danos aos rins e ao fígado, e estimulação da medula óssea para aumentar a produção de plaquetas sanguíneas. A exposição a baixos níveis de 10 ppm pode produzir efeitos de envenenamento crônico no sistema nervoso central. A ingestão do líquido pode produzir os mesmos sintomas mencionados acima. Contato com a pele pode causar dermatite. O vapor é irritante para os olhos, nariz e pulmões. Devido ao seu forte odor desagradável, há sempre um aviso suficiente contra qualquer superexposição. Uma concentração de 10 ppm é questionável para os seres humanos. Valor LCLO, inalação (ratos): 4000 ppm/4 h Valor LD50, oral (ratos): 1500 mg/kg. Huh e colaboradores (1986) investigaram o efeito do ácido glicirretínico na toxicidade da piridina em camundongos. O pré-tratamento com ácido glicirretínico diminuiu a depressão do sistema nervoso central e a mortalidade em animais induzida pela piridina. Esse pré-tratamento diminuiu acentuadamente a atividade da enzima transaminase sérica e aumentou a atividade da anilina hidroxilase microssomal hepática [9012-90-0], uma enzima que metaboliza a piridina. |
| Inflamabilidade e Explosibilidade | A piridina é um líquido altamente inflamável (classificação NFPA=3) e seu vapor pode viajar uma distância considerável e "retornar". O vapor de piridina forma misturas explosivas com o ar em concentrações de 1,8 a 12,4% (em volume). Extintores de dióxido de carbono ou pó químico seco devem ser usados para incêndios de piridina. |
| Usos industriais | A piridina é um bom solvente para um grande número de compostos, tanto orgânicos quanto inorgânicos (Windholz et al 1983). Cerca de 50% da piridina utilizada nos EUA é para a produção de produtos químicos agrícolas, como os herbicidas paraquat, diquat e triclopyr e o inseticida clorpirifós. Outros usos são na produção de piperidina; a fabricação de produtos farmacêuticos, como esteróides, vitaminas e anti-histamínicos; e como solvente. Os usos de solventes são encontrados nas indústrias farmacêutica e de resinas de policarbonato. É particularmente útil como solvente em processos onde o HC1 é desenvolvido (Santodonato et al 1985). Os usos menores da piridina são para a desnaturação de misturas de álcool e anticongelantes, como auxiliar de tingimento em têxteis e como agente aromatizante (Jori et al 1983; Furia 1968; HSDB 1988). |
| Alérgenos de contato | A piridina (piridina não substituída) e seus derivados (piridinas substituídas) são amplamente utilizados em química. A piridina é um solvente usado para muitos compostos orgânicos e sais químicos anidros metálicos. Contido no reagente Karl Fischer, induziu dermatite de contato em técnico de laboratório. Nenhuma sensibilidade cruzada é observada entre essas diferentes substâncias. |
| Perfil de segurança | Veneno por via intraperitoneal. Moderadamente tóxico por ingestão, contato com a pele, vias intravenosa e subcutânea. Levemente tóxico por inalação. Irritante grave para a pele e os olhos. Dados de mutação relatados. Pode causar depressão do sistema nervoso central, distúrbios gastrointestinais e danos ao fígado e aos rins. Um líquido inflamável e perigoso risco de incêndio quando exposto ao calor, chamas ou oxidantes. Grave risco de explosão na forma de vapor quando exposto a chamas ou faíscas. Reage violentamente com ácido clorossulfônico, trióxido de cromo, tetróxido de dinitrogênio, HNO3, oleum, percromatos, ppropiolactona, AgClO4, H2SO4. Reação incandescente com flúor. Reage formando produtos pirofóricos ou explosivos com trifluoreto de bromo e hipofluorito de trifluorometila. Misturas com formamida + iodo + trióxido de enxofre são perigosas no armazenamento, liberando dióxido de carbono e ácido sulfúrico. Incompatível com materiais oxidantes. Reage com anidrido maleico (acima de 150 graus) evoluindo dióxido de carbono. Para combater o fogo, utilize espuma de álcool. Quando aquecido até a decomposição, emite vapores altamente tóxicos de NOx. |
| Exposição potencial | A piridina é utilizada como solvente na indústria química e como desnaturante do álcool etílico; como intermediário na produção de pesticidas; em produtos farmacêuticos; na fabricação de tintas, explosivos, corantes, borracha, vitaminas, sulfas; e desinfetantes. |
| Carcinogenicidade | A piridina não foi carcinogênica em vários estudos subcutâneos crônicos. Ratos F344 receberam piridina por via oral na água potável em doses de 0, 7, 14 ou 33 mg/kg por 2 anos. A dose máxima produziu uma diminuição no peso corporal e no consumo de água. Aumento de adenoma ou carcinoma tubular renal e hiperplasia tubular foram observados em homens com 33 mg/kg. Foi observado aumento da leucemia de células mononucleares em fêmeas com 14 e 33 mg/kg, o que foi considerado equívoco em termos da relação com a exposição à piridina, uma vez que este é um achado comum nesta estirpe de ratos. Alterações não neoplásicas relacionadas à concentração no fígado foram observadas com 33 mg/kg. Ratos Wistar machos foram tratados de forma semelhante com doses de 0, 8, 17 ou 36 mg/kg durante 2 anos. A diminuição da sobrevivência e do peso corporal foi observada com 17 e 36 mg/kg. Aumento de adenomas de células testiculares foi observado com 36 mg/kg. Não foram notificadas alterações na sobrevivência ou nas taxas de neoplasia noutros tecidos, incluindo o rim, embora tenha sido observado aumento da nefropatia e degeneração/necrose centrolobular hepática em alguns ratos tratados com piridina. |
| Fonte | A piridina ocorre naturalmente em batatas, anabasis, folhas de meimendro, hortelã-pimenta (0 a 1 ppb), folhas de chá e folhas de tabaco (Duke, 1992). Identificado como um dos 140 constituintes voláteis em óleos de soja usados coletados de uma planta de processamento que fritava vários produtos de carne bovina, frango e vitela (Takeoka et al., 1996). |
| Destino ambiental | Biológico.Heukelekian e Rand (1955) relataram um valor de DBO 5-d de 1,31 g/g, que é 58,7% do valor ThOD de 2,23 g/g. A Nocardia sp. isolado do solo foi capaz de transformar a piridina, na presença de semicarbazida, em um produto intermediário identificado como semialdeído do ácido succínico (Shukla e Kaul, 1986). 1,4-dihidropiridina, dialdeído glutárico, semialdeído de ácido glutárico e ácido glutárico foram identificados como produtos intermediários quando a piridina foi degradada pela cepa Z1 de Nocardia (Watson e Cain, 1975). Fotolítico.A irradiação de uma solução aquosa a 50 graus durante 24 horas resultou num rendimento de 23,06% de dióxido de carbono (Knoevenagel e Himmelreich, 1976). Químico/Físico.A reação em fase gasosa do ozônio com piridina em ar sintético a 23 graus produziu um sal nitrado com a fórmula: [C6H5NH]+NO3 - (Atkinson et al., 1987). A ozonização da piridina em soluções aquosas a 25 graus foi estudada com e sem a adição de álcool terc-butílico (20 mM) como eliminador de radicais. Com álcool terc-butílico, a ozonização da piridina rendeu principalmente N-óxido de piridina (rendimento de 80%), que era muito estável em relação ao ozônio. Sem álcool terc-butílico, o anel heterocíclico é rapidamente clivado formando amônia, nitrato e o composto amídico ácido N-formil oxâmico (Andreozzi et al., 1991). |
| Metabolismo | A piridina é absorvida pelo trato gastrointestinal, pele e pulmões e é eliminada pela urina, fezes, pele e pulmões, tanto como metabólitos quanto como composto original (Jori et al 1983). A captação pelos tecidos aumenta com a dose e a eliminação é de natureza bifásica (Zharikov e Titov 1982; HSDB 1988). A eliminação é rápida e parece não haver acúmulo de tecido (Jori et al 1983). A observação por His (1887) da excreção urinária de Af-metilpiridina por animais doseados com piridina foi o primeiro exemplo de metilação de Af. Os metabólitos urinários conhecidos da piridina em mamíferos agora incluem N-óxido de piridina, N-metil piridina, 4-piridona, 2-piridona e 3-hidroxipiridina. Alguns metabólitos ainda precisam ser identificados (Damani et al 1982). As quantidades relativas dos metabólitos são altamente dependentes da espécie e da dose (Gorrod e Damani 1980). Por exemplo, foi demonstrado que o rato excreta 70% de uma dose de 1 mg/kg na urina nas primeiras 24 horas após a administração, mas esse número cai para apenas 5,8% para uma dose de 500 mg/kg (D'Souza et. em 1980). Embora a excreção urinária de piridina e seus metabólitos pareça ser a principal via de eliminação, a excreção não urinária não foi extensivamente estudada (Santodonato et al 1985). Em coelhos, a atividade da piridina N-metiltransferase demonstrou ser mais alta no citosol pulmonar e descobriu-se que utiliza 5-adenosil metionina como doador de metil (Damani et al 1986). Esta via é saturável tanto no rato quanto na cobaia (D'Souza et al 1980). O produto desta reação, N-metil piridina, é menos cronicamente tóxico, mas mais agudamente tóxico que a piridina (Williams 1959). O N-óxido de piridina é produzido pelo sistema citocromo P-450 e a atividade é induzida pelo pré-tratamento com fenobarbital ou piridina, mas não pelo 3-metilcolantreno (Gorrod e Damani 1979; Kaul e Novak 1987). No coelho, o induzível por álcool (e induzível por piridina) P-450 LM3Aparece ser o baixo Kmisozima que catalisa a produção de óxido Af de piridina (Kim e Novak 1989). A N-oxidação da piridina pode representar uma via de bioativação (Santodonato et al 1985) e esta via torna-se mais importante à medida que a dose de piridina é aumentada (Damani et al 1982). |
| armazenar | A piridina deve ser usada apenas em áreas livres de fontes de ignição, e quantidades superiores a 1 litro devem ser armazenadas em recipientes metálicos hermeticamente fechados em áreas separadas dos oxidantes. |
| Envio | UN1992 Líquidos inflamáveis, tóxicos, nos, Classe de perigo: 3; Rótulos: 3-Líquido inflamável, 6.1-Materiais venenosos, Nome técnico obrigatório. |
| Métodos de Purificação | As impurezas prováveis são H2O e aminas, como picolinas e lutidinas. A piridina é higroscópica e miscível com H2O e solventes orgânicos. Pode ser seco com KOH sólido, NaOH, CaO, BaO ou sódio, seguido de destilação fracionada. Outros métodos de secagem incluem repouso em peneiras moleculares Linde tipo 4A, CaH2 ou LiAlH4, destilação azeotrópica do H2O com tolueno ou *benzeno, ou tratamento com brometo de fenilmagnésio em éter, seguido de evaporação do éter e destilação da piridina. Um método recomendado [Lindauer Mukherjee Pure Appl Chem 27 267 1971] seca a piridina sobre KOH sólido (20g/Kg) por 2 semanas e destila fracionadamente o sobrenadante sobre peneiras moleculares Linde tipo 5A e KOH sólido. O produto é armazenado sob nitrogênio2-livre de CO. A piridina pode ser armazenada em contato com BaO, CaH2 ou peneiras moleculares. Os materiais não básicos podem ser removidos por destilação a vapor de uma solução contendo 1,2 equivalentes de 20% de H2SO4 ou 17% de HCl até que cerca de 10% da base tenha sido transportada junto com as impurezas não básicas. O resíduo é então alcalinizado e a base é separada, seca com NaOH e destilada fracionadamente. Alternativamente, a piridina pode ser tratada com agentes oxidantes. Assim, a piridina (800mL) foi agitada durante 24 horas com uma mistura de sulfato cérico (20g) e K2CO3 anidro (15g), depois filtrada e destilada fracionadamente. Hurd e Simon [J Am Chem Soc 84 4519 1962] agitaram piridina (135mL), água (2,5L) e KMnO4 (90g) por 2 horas a 100o, depois permaneceram por 15 horas antes de filtrar os óxidos de manganês precipitados. A adição de KOH sólido (cerca de 500 g) causou a separação da piridina. Foi decantado, refluxado com CaO por 3 horas e destilado. A separação da piridina de alguns dos seus homólogos pode ser conseguida por cristalização dos oxalatos. A piridina é precipitada como seu oxalato adicionando-a à solução agitada de ácido oxálico em acetona. O precipitado é filtrado, lavado com acetona fria e a piridina é regenerada e isolada. Outros métodos baseiam-se na formação de complexos com ZnCl2 ou HgCl2. |
| Incompatibilidades | Reação violenta com oxidantes fortes; ácidos fortes; ácido clorossulfônico; anidrido maleico; óleo iodo. |
| Depósito de lixo | Incineração controlada pela qual os óxidos de nitrogênio são removidos do gás efluente por purificadores, dispositivos catalíticos ou térmicos. |
| Produtos e matérias-primas para preparação de piridina |
| Matérias-primas | Sulfuric acid-->Ammonia-->Benzene-->COAL TAR-->3-Picoline-->COKEOVENGAS-->1,5-DIIDROCLORETO DE DIAMINOPENTANO |
| Produtos de preparação | Methyl 2-Fluoroisonicotinate-->2-ACETYL-5-CYANOTHIOPHENE-->5-BROMO-2-FLUOROCINNAMIC ACID-->4-NITROISOPHTHALIC ACID-->3,5-DIMETHOXYCINNAMIC ACID-->2-(2-Butoxyethoxy)ethyl acetate-->2,4-MESITYLENEDISULFONYL DICHLORIDE-->(4-FLUORO-BENZYL)-METHYL-AMINE-->1-Phenacylpyridinium bromide-->3-(TRIFLUOROMETHOXY)CINNAMIC ACID-->trans-Ferulic acid-->3-(Trifluoromethyl)pyrazole-->4-Fluorocinnamic acid-->Indigosol Green Blue IBC-->2-Amino-4-methyl-5-acetylthiazole-->Benzyl 2-chloroacetate-->5-ACETAMIDONICOTINIC ACID-->7-ACETOXYCOUMARIN-->2-AMINO-4-METHYL-QUINOLINE-3-CARBONITRILE-->N-PHENYLISONICOTINAMIDE-->Allyl methyl carbonate-->Pyridine-3-sulfonyl chloride hydrochloride-->Syringaldehyde-->2,4,5,6-TETRAMETHYLBENZENEDISULFONYL DICHLORIDE-->3-(3-METHYL-2-THIENYL)ACRYLIC ACID-->Vat Grey M-->17beta-Hydroxy-17-methylandrosta-4,9(11)-dien-3-one-->butyl N-phenylcarbamate-->3-Methoxycinnamic acid-->1-CHLORO-2-METHYLPROPYL CHLOROFORMATE-->Pyrazinecarbonitrile-->2-AMINO-6-CHLORO-3,5-DICYANOPYRIDINE-->4-BROMO-TETRAHYDROPYRAN-->Phenylcarbamic acid propyl ester-->Hydrocortisone acetate-->5-METHYLPICOLINIC ACID-->4-Acetamido-2-chloropyridine-->Pyridinium p-Toluenesulfonate-->1,2,4-Triazolo[4,3-a]pyridin-3(2H)-one-->Dicloreto de paraquate |
Tag: piridina, fabricantes, fornecedores, fábrica de piridina na China
Você pode gostar também
-

Preço competitivo CAS 624-89-5 Sulfeto de Metil Etil
-

CAS 1335-66-6 da fábrica chinesa isociclocitral
-

Venda de fábrica CAS 100-06-1 4-Metoxiacetofenona
-

Aditivos alimentares de qualidade alimentar CAS 93-92-5 acetato de estiralila
-

Preço de fábrica Melhor preço CAS 577-16-2 2-Metilacetofenona
-

2-Etoxinaftaleno
Enviar inquérito

